¿Qué es la ISO 15189?
📌La ISO 15189 (Laboratorios clínicos) es la norma más importante relacionada con la calidad y competencia para laboratorios clínicos y médicos, cuyo objetivo es garantizar que los resultados sean confiables, precisos y trazables, lo que impacta directamente en la seguridad del paciente y la toma de decisiones médicas.
Descubre sus beneficios
¿A quién aplica la norma ISO 15189?
🌍La norma ISO 15189 aplica a todos los laboratorios clínicos, con independencia de si son públicos o privados.
Hospitales
Laboratorios
Bancos de sangre
La norma ISO 15189 NO es obligatoria, y por tanto, es tu decisión obtenerla y beneficiarte de ella.
Sin embargo, en muchas ocasiones, puede estar solicitada por el Ministerio de Sanidad o autoridades nacionales para acreditaciones (contratos públicos, licitaciones), asociaciones médicas, seguros de salud o por organismos reguladores.
Los 6 pasos para certificarte en ISO 15189
A continuación te dejo las claves para conseguir la certificación iso 15189. Si sigues estos pasos, no te costará en absoluto superar la auditoría externa que lo otorga.
1. Diagnóstico inicial
Para superar este paso, es necesario analizar la situación del laboratorio para conocer su punto de partida y establecer la política de calidad sobre la que se apoyará todo el sistema.
En esta etapa se analizan también las políticas y prácticas vigentes, como protocolos de bioseguridad, criterios de aceptación de muestras, procesos de análisis y entrega de resultados, además de evaluar los riesgos en las fases preanalítica, analítica y post-analítica. La política que guía este diagnóstico debe enfocarse en garantizar la calidad y fiabilidad de los resultados clínicos, la seguridad tanto del paciente como del personal, el cumplimiento normativo y la mejora continua.
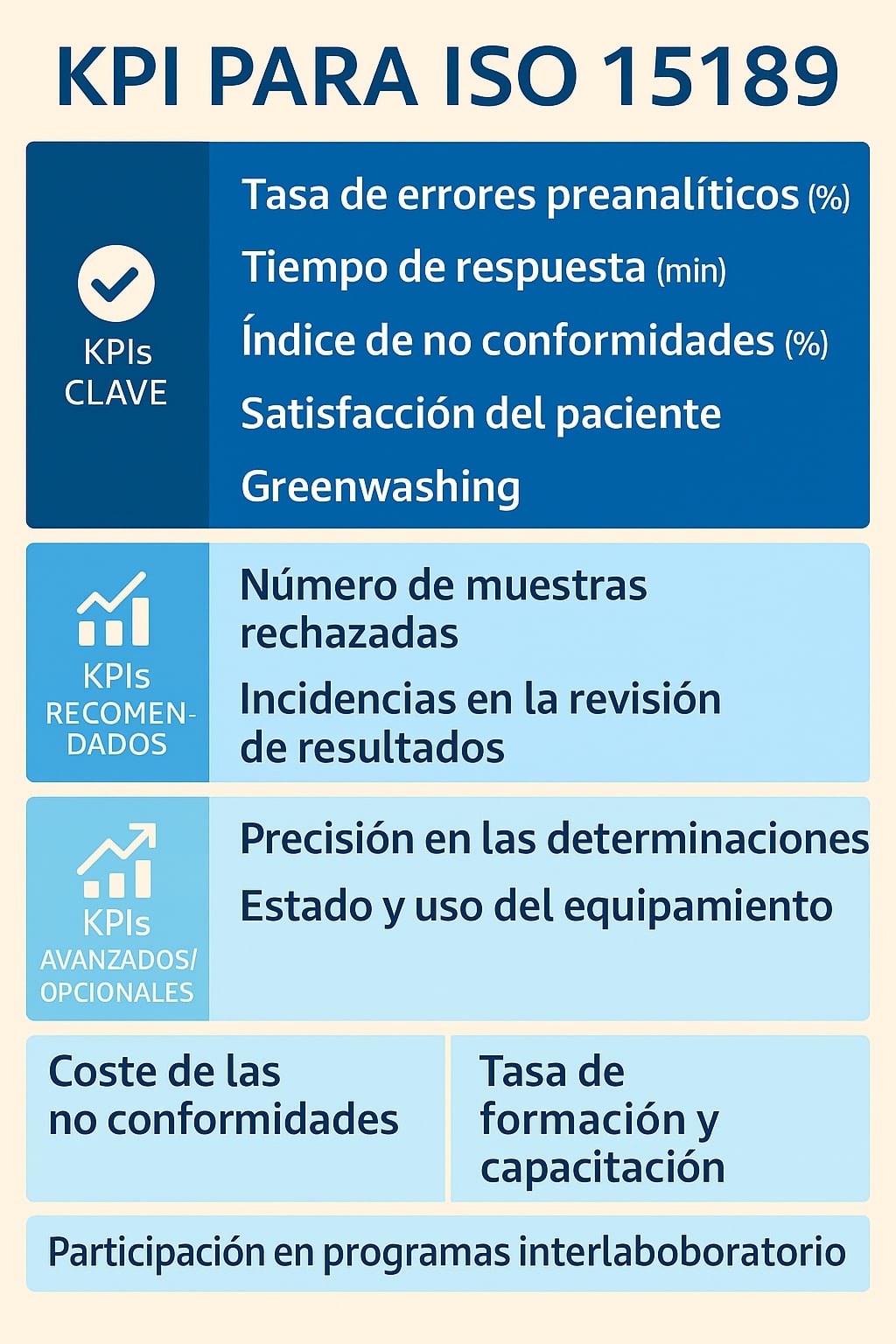
Deben establecerse indicadores, ya que la norma exige metas claras y cuantificables, aunque estos variarán según el contexto de cada organización:
Además, se deben evaluar los posibles riesgos teniendo en cuenta la diversidad de las causas:
2. Planificación
En esta etapa, se ponen definen todos los objetivos a los que hemos hecho alusión en el apartado anterior.
Serán la base de la planificación, ya que todos los esfuerzos deben ir en esa dirección, y todos ellos conformarán la «hoja de ruta» para maximizar la calidad, la fiabilidad y eficiencia de los ensayos. Se debe de evaluar posibles riesgos, así como proporcionar una correcta asignación de roles y la inversión necesaria.
Deberá existir una división del trabajo y de las responsabilidades clara, con la inclusión de distintos equipos especializados (producción, seguridad, documentación y trazabilidad, validación, etc…) y un Responsable de Calidad encargado de que se mantiene la fiabilidad.
Para lograr que plan de acción sea un éxito, se debe hacer hincapié en los siguientes aspectos:

Ejemplo:
Un laboratorio clínico especializado en análisis de biología molecular detecta que el 25 % de las desviaciones registradas en auditorías internas se deben a fallos en la gestión de muestras y ausencia de control en la cadena de custodia. Se establece implantar un sistema digital de trazabilidad de muestras con códigos de barras únicos y registro automático en la base de datos antes de finalizar el tercer trimestre. Además, se definirá un procedimiento estandarizado de control documental que permita acceder a los historiales de cada muestra. Para ello, se asigna un presupuesto de 75.000 € y un equipo multidisciplinar formado por 2 técnicos de laboratorio, 1 bioinformático y 1 responsable de calidad, bajo la dirección del Responsable Técnico del laboratorio.
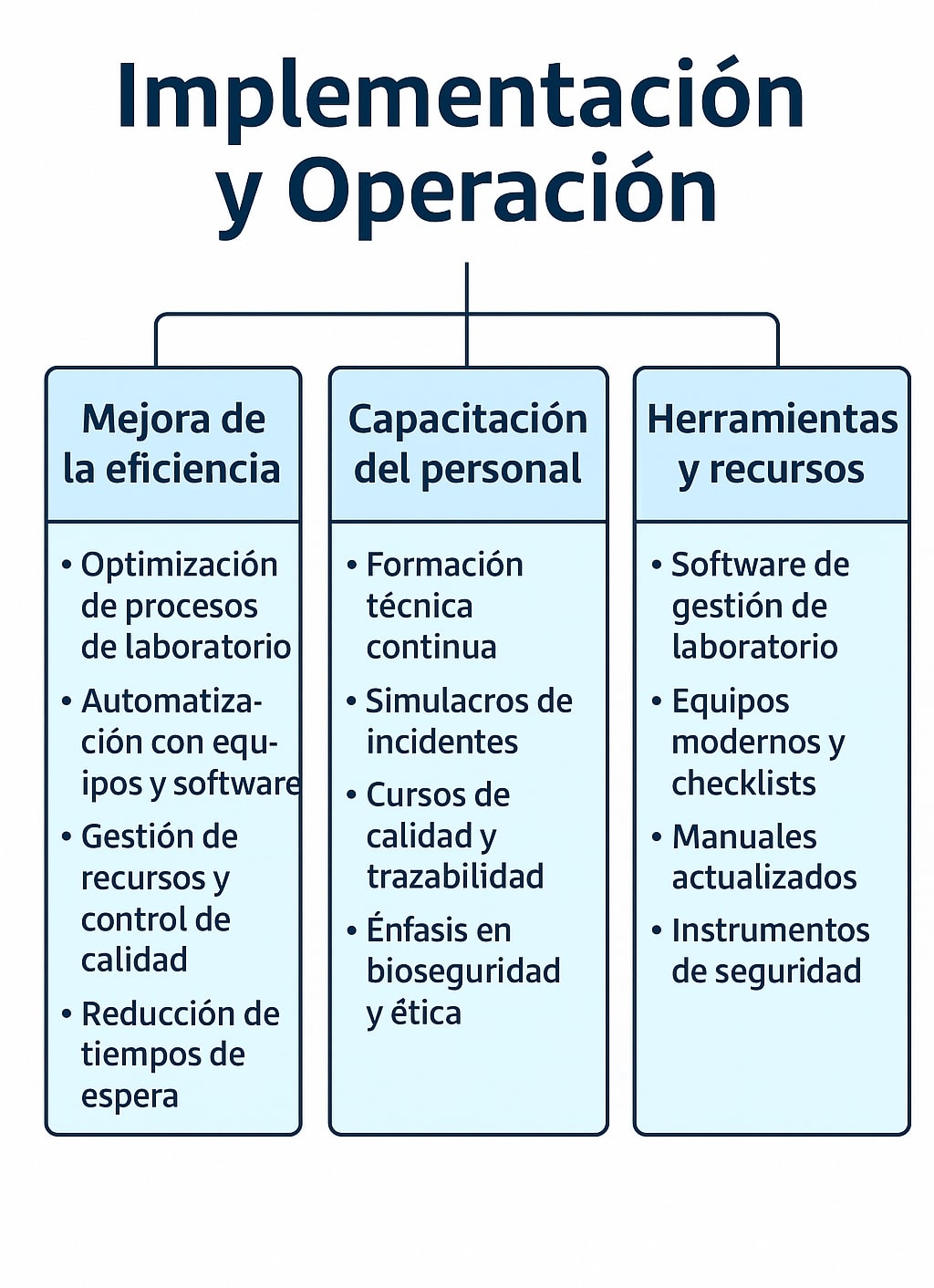
3. Implementación y Formación del personal
Cuando ya está creado el plan de acción, sólo queda ponerlo en marcha. Una buena implementación en el día a día permitirá superar la auditoría con facilidad.
Por ejemplo, para aumentar la calidad de los laboratorios, se implementarán zonas limpias con control de acceso y vestimenta apropiada, control y monitorización de partículas y agentes microbiológicos, y procesos estrictos de limpieza y desinfección de maquinaria de forma periódica.
En cuanto a capacitar al personal, por ejemplo, se fijarán cursos de formación técnica para los trabajadores, formación en trazabilidad de lotes y simulación de incidentes (por ejemplo: fallo en cadena de frío, contaminación cruzada de muestras).
Como ejemplo, para proporcionar herramientas y recursos, se proporcionarán instalaciones adecuadas para la mejora de la fiabilidad y la eficiencia, se podrán adquirir softwares de gestión de laboratorio (STARLIMS, LabVantage, LabWare, QBench…). También se asegurará la calibración de los equipos y checklists digitales. Además se crearán boletines donde se informe de los avances, para reforzar la cultura de mejora continua.
4. Seguimiento y Medición
Para estar seguros de que la ISO 15198 llega para quedarse, es necesario que todos los trabajadores de la empresa la adopten de la forma más sencilla y práctica posible. Para evaluar su efectividad y garantizar que sus objetivos se cumplen:
- Monitoreo constante: Implantar sistemas de control interno de calidad (IQC) para cada análisis, evaluando la exactitud y precisión de los resultados, así como recurrir al uso de controles externos.
- Análisis de resultados, revisando métricas clave para evaluar el buen funcionamiento. ¿Se cumplen las expectativas de los clientes? ¿Se observa una disminución en el número y gravedad de incidencias? ¿Se ha aumentado la eficiencia?
- Ajustes y mejoras continuas: Reforzar la formación, reasignar recursos, optimizar procesos de soporte o actualizar herramientas si se detecta que los resultados no cumplen los objetivos.
5. Auditoría interna
Esta paso consiste en simular la auditoría externa que otorga la certificación, de forma que se pueda evaluar la calidad de los cambios. Si la empresa supera la auditoría interna fácilmente, le costará poco esfuerzo superar la externa y obtener la certificación.
Lo ideal sería planificar una serie de auditorías de todo el proceso de los ensayos clínicos, y redactar un informe con los resultados observados. Con ello, se logran identificar áreas de mejora, y permiten mostrar a la empresa auditora los progresos sistemáticos. También se evalúa si los registros y mediciones son completos y trazables.
Para realizar la auditoría interna, diseña preguntas modelo que permitan «examinar» de forma interna a la plantilla. De esta forma, podrás comprobar qué puntos necesitan mejorar.
6. Auditoría externa (Certificación)
La ISO 15189, exige que la certificación sea emitida por una empresa acreditada externa (AENOR, TÜV, SGS, Bureau Veritas…). Para ello, deberás recabar información sobre las opciones que tengas y ponerte en contacto para recibir un presupuesto.
Una vez hayas contratado el servicio, deberás superar la auditoría externa para obtener la certificación. Si se detectan algunos errores, se otorgará el período de 30 días para solucionarlos.
💡Será sencillo pasar el período de auditoría externa, si se utilizan las auditorías internas como simulaciones reales. De esta forma, el personal estará más preparado y relajado.
💡La certificación ISO 15189 se entrega por un período de 3 años, con revisiones periódicas para confirmar el mantenimiento de las mejoras. Por ello, es necesario garantizar que la empresa sigue activamente alineada con la norma.
